第一作者简介:杨杰(1988- ),男,安徽淮南人,硕士研究生,从事森林土壤质量与环境学研究。E-mail:jiey179@163.com
*通信作者简介:姜培坤(1963- ),男,浙江桐乡人,教授,主要从事土壤质量与环境学研究。E-mail:jiangpeikun@zafu.edu.cn
植硅体碳(phytolith-occluded organic carbon, PhytOC)具有很强的抗风化能力,能存在于土壤中达数千年之久,成为陆地土壤长期固碳的重要机制。论文以中国亚热带地区苦竹( Pleioblastus amarus)林生态系统为对象,探究硅、植硅体及植硅体碳在竹林生态系统中的分布特征。研究结果表明,植硅体碳广泛分布于苦竹地上部分各器官中,植硅体和植硅体碳含量均为叶>枝>秆。被传统植硅体研究所忽略的竹枝和竹秆中的植硅体碳储量占到地上部分植硅体碳总储量的7.2%和51.1%。植硅体碳占总有机碳的比例在叶、枝、秆中分别为0.59%、0.21%和0.28%,植硅体碳占总有机碳的比例因积累器官的不同而存在明显的差异。植物体内植硅体的含量与土壤中植物可利用硅的含量之间存在显著的线性相关关系( R2= 0.91, P< 0.05),而与土壤中总硅无相关性( R2 = 0.16, P> 0.05)。苦竹林植硅体碳封存速率为40.2 kg·hm-2·a-1。
Phytolith-occluded organic carbon (PhytOC) can exist in the soil for thousand years, thus it is an important mechanism of long-term carbon sequestration in soils. In this study, Pleioblastus amarus forest in subtropical China was selected as experimental materials to discuss the distribution of silicon, phytolith, and PhytOC in a Pleioblastus amarus forest system. A microwave digestion method was used in this study to isolate phytolith from plant material and soil samples, and the PhytOC were determined by alkali dissolution-spectrophotometry method. The results showed that the contents of phytolith and PhytOC in a Pleioblastus amarus forest system decreased in the order: leaf > branch > culms. For different organs, there was significant linear correlation between Si content and phytolith content ( R2 = 0.98, P< 0.01), and between phytolith content and PhytOC content ( R2 = 0.52, P< 0.01), and there was significant negative linear correlation between total organic carbon content and PhytOC content ( R2 = 0.57, P < 0.01), and between organic carbon content in phytolith and phytolith content ( R2 = 0.17, P< 0.01). The PhytOC stocked in branches and culms accounted for 17.2% and 51.1% of total PhytOC stock in above-ground part, respectively. PhytOC stocked in leaves, branches and culms accounted for 0.59%, 0.21% and 0.28% of total organic carbon stock, respectively. The ratios of PhytOC/total organic carbon greatly varied in different organs. The phytolith contents in bamboo plants were linearly correlated with plant-available Si contents in the soil ( R2 = 0.91, P< 0.05), but poorly correlated with total Si contents in the soil ( R2 = 0.16, P> 0.05). The PhytOC production rate in the Pleioblastus amarus forest system studied was 40.2 kg·hm-2·a-1.
土壤碳库容量巨大, 但由于土地利用方式的不确定性、碳存储机制的复杂性和环境条件的不断变化, 绝大部分土壤有机碳都不能够长期稳定存在[1]。找到一种可以使土壤有机碳长期稳定存在的碳封存机制具有重要意义。
植硅体(phytolith)是在植物生长过程中, 通过根系吸收的无定型硅酸[Si(OH)4]经维管束输送后在植物细胞内腔或细胞间隙中形成的硅包碳化合物[2]。植硅体几乎存在于所有植物体中, 特别是在禾本科中的竹亚科植物中含量尤其丰富[3]。植硅体碳是一种在植硅体形成过程中被包裹于植硅体内的有机碳[4], 随植硅体进入土壤后, 可以稳定存在数千年甚至上万年之久[5], 成为陆地土壤长期碳封存的重要机制之一。这种长期的生物地球化学碳封存形式被认为在减少大气中二氧化碳的含量、缓解温室效应方面具有很大的潜力[6, 7]。
竹亚科植物是一类对土壤中的硅有很强富集能力的植物[8]。全球竹林面积达2 200× 104 hm2, 中国分布约720× 104 hm2 [9]。在竹林植硅体碳汇的相关研究中, Parr等[3]、Song等[10]和Li等[9]已经通过竹叶对竹林固碳能力进行简单估测, 但由于竹枝和秆等器官的植硅体及植硅体碳含量较低[11], 给植硅体碳的准确测定带来了一定的困难, 因此很少有涉及到枝、秆等器官的研究报道。植硅体碳储量决定于植硅体碳的含量和生物量两个因素[3, 10], 虽然竹类植物枝和秆中植硅体碳含量不高[11], 但因其生物量巨大[12], 在计量竹林地上部分植硅体碳总储量时, 竹枝和秆可能是一个不可忽视的、重要的部分, 值得研究。
苦竹(Pleioblastus amarus)是一种笋、材、药三用竹种, 具有很大的经济价值, 同时苦竹还是一种介于丛生竹与散生竹之间的竹种资源, 对环境的适应性很强, 广泛分布于我国南方各省及长江中下游地区, 并且有研究表明苦竹在生长过程中既体现丛生竹的生长特性, 也体现散生竹的生长特性[13], 因此本研究以苦竹为研究对象, 对地上不同器官中硅、植硅体和植硅体碳进行测定, 以揭示其在地上不同器官中的分布和差异。同时, 对于一个完整的生态系统来说, 植被系统固定的植硅体碳最终都将归还、封存于土壤中[14], 本文进一步研究了土壤中植硅体碳的储量和分布规律, 为我国竹林生态系统植硅体碳研究提供依据。
研究区选在浙江省杭州市余杭区(30° 09′ ~30° 34′ N, 119° 40′ ~120° 23′ E), 海拔在150~200 m之间, 属北亚热带季风气候区, 年平均气温18.4 ℃, 年平均降水量1 378.5 mm。母质为凝灰岩, 土壤为红壤土类, 黄红壤亚类。竹林为当地典型笋材兼用林, 每年4— 5月施肥(N: P2O5: K2O = 15: 15: 15, 0.75 t· hm-2), 每年秋季砍去6 a生以上的老竹。
2013年8月在研究区内选取4处坡向不同且竹林生长较均匀的中坡建立采样点, 设置20 m× 20 m的标准样地。统计每个标准样地内不同年龄竹子的数量并量取胸径, 选取每个标准样地每个竹龄中与平均胸径相等的竹子为标准样株, 采伐整株标准竹, 并测量标准样株不同器官的生物量, 各器官分取200~500 g带回实验室烘干, 粉碎, 进行相关指标分析测定。同时, 在4个标准样地内, 每个标准样地随机选取三个点, 挖取土壤剖面, 分别采取0~5、5~10、10~20、20~30、30~40、40~50、50~60、60~70、70~80以及80 cm以下不同土层的土壤, 再将三个点相同土层的土壤混合成一个土壤样品挑去根及枯枝落叶带回实验室进行分析测定。容重的采集与土壤分析样品采集同时进行。
1.3.1 植物样品的分析
植物样品在分析测定前, 用超纯水洗净, 70 ℃烘干, 粉碎(< 0.5 mm)。样品植硅体的提取采用微波消解法[15], 之后用0.800 0 mol· L-1的重铬酸钾溶液对植硅体进行检验, 确保植硅体表面有机物质完全被去除[16], 提取后的植硅体于65 ℃的烘箱中烘干48 h, 称重。植硅体碳的测定采用碱溶分光光度法[17], 在样品测定的同时加入土壤标准样(GBW07405)及植物标准样(GBW07602)对测定的准确性进行检验, 每个样品重复3次。
1.3.2 土壤样品的分析
土壤pH值的测定水土比为5: 1, 土壤总有机碳的测定采用浓硫酸-重铬酸钾氧化 法[18], 土壤总硅及总磷的测定采用偏硼酸锂熔融-比色法[19], 土壤植硅体的提取先采用微波消解法, 再用比重为2.35和1.60 g· mL-1的ZnBr2重液除去残余的土壤及杂质[20]。土壤植硅体碳测定的方法与植物相同。土壤中植物可利用硅的提取采用CaCl2浸提-硅钼蓝比色法[21]。
数据处理使用SPSS 18.0系统进行统计分析, Duncan新复极差法测验不同处理的差异显著性; Origin 8.5作图。
研究结果表明(表1), 总硅在地上部分各器官中含量变化的顺序为:叶> 枝> 秆, 不同年龄段的竹叶之间硅含量变化范围为13.57± 1.27~19.77± 3.03 g· kg-1, 平均含量16.84 g· kg-1; 苦竹枝中硅含量变化范围为11.24± 2.97~15.65± 0.48 g· kg-1, 平均含量为14.10 g· kg-1; 苦竹秆中, 硅含量最低的为两年生竹, 含量为1.63± 0.34 g· kg-1, 最高为5年生, 含量为5.05± 0.75 g· kg-1, 平均含量3.13 g· kg-1。3种器官中, 仅秆中硅含量在不同年龄竹之间具有显著差异性(P=0.05, 表1)。
| 表1 不同年龄不同器官中硅、总有机碳、植硅体、植硅体封存有机碳和植硅体碳的含量 Table 1 Content of Si, total carbon (TC), phytolith, organic carbon (OC) content in phytolith and PhytOC in organs of different ages (g· kg-1) |
植硅体含量在地上部分各器官中的变化趋势与硅相同, 竹叶中植硅体含量变化范围在31.46± 5.43~45.56± 5.71 g· kg-1之间, 平均含量37.35 g· kg-1。对于不同年龄段的枝来说, 植硅体的含量变化不太明显, 为23.77± 4.45~32.82± 2.79 g· kg-1, 平均含量27.99 g· kg-1。秆中植硅体的含量也是最低的, 最低含量为4.66± 0.70 g· kg-1, 最高含量8.58± 1.93 g· kg-1, 平均含量6.51 g· kg-1。所有器官中, 植硅体含量在不同年龄竹之间均无显著差异性(P= 0.05, 表1)。
在植物地上部分各器官之间, 植硅体封存有机碳含量总体变化趋势为:秆> 叶> 枝, 其中不同年龄段的竹叶之间植硅体封存有机碳的含量存在微小的变化, 变化范围在 85.6± 17.7~103.6± 12.0 g· kg-1之间, 平均含量97.4 g· kg-1。植硅体封存有机碳含量在不同年龄段的枝中变化从50.2± 11.2到95.3± 21.5 g· kg-1不等, 平均含量为65.3 g· kg-1。不同年龄段的秆封存植硅体有机碳含量差异较大, 其中含量最低为63.9± 16.9 g· kg-1, 含量最高为295.6± 40.0 g· kg-1, 平均含量165.5 g· kg-1(表1)。在叶、枝、秆三种植物器官中, 植硅体封存有机碳的含量在不同竹龄竹枝和秆之间均存在显著差异(P=0.05, 表1), Si、植硅体和植硅体封存有机碳含量在不同竹龄竹叶中均无显著差异(表1)。
不同器官之间植硅体和植硅体碳的含量变化趋势大致相同, 竹叶中植硅体碳的含量变化范围在2.43± 0.21~4.38± 0.38 g· kg-1之间, 平均含量3.50 g· kg-1; 枝的植硅体碳含量变化范围为1.32± 0.21~2.11± 0.53 g· kg-1, 平均含量1.70 g· kg-1; 秆中植硅体碳的含量最低(0.38± 0.18~1.48± 0.17 g· kg-1), 平均含量1.04 g· kg-1(表1)。
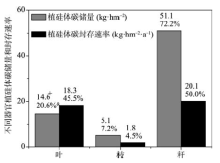
每公顷苦竹林地上部分植硅体碳总储量为83.7 kg, 叶枝秆共储存70.7 kg。植硅体碳储量在不同器官中变化的顺序为秆(51.1 kg· hm-2)> 叶(14.6 kg· hm-2)> 枝(5.1 kg· hm-2), 竹叶中植硅体碳储量远小于竹枝和秆的总储量(表2)。
| 表2 苦竹林总碳(土壤有机碳)、植硅体和植硅体碳储量 Table 2 Storage of TC (SOC), phytolith and PhytOC in Pleioblastus amarus forest |
土壤中总硅的含量变化范围在55.67~58.70 g· kg-1之间, 不同土层之间硅含量的变化并不明显。对于土壤中植物可利用硅来说, 5~10 cm土层含量最高, 为15.10 g· kg-1, 80~90 cm土层含量最低, 为4.03 g· kg-1, 在10~30 cm和40~80 cm土层中不断增加(图1)。
土壤中植硅体含量的变化范围在6.69~32.08 g· kg-1之间, 变化趋势与植物可利用硅变化趋势大致相同, 40~50 cm土层中植硅体含量最低, 在70~80 cm土层中植硅体含量最高。在土壤表土层(0~10 cm土层)中无论是植物可利用硅还是植硅体的含量都很高, 在0~50 cm土层中随着深度的增加呈现出有规律的减少特征, 在50~80 cm土层中, 随着深度的增加植硅体及植物可利用硅的含量有所增加(图1)。
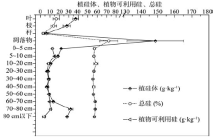 | 图1 不同土层中植硅体、总硅和植物可利用硅的分布Fig. 1 Distribution of phytolith, total SiO2 and plant-available Si at different soil depths (n=4) |
植硅体碳含量随着土层的加深而不断变化, 含量最高为0.091 g· kg-1, 最低为0.033 g· kg-1。随土层不断加深, 不同土层中植硅体碳占总有机碳的比例从0.25%不断增加到0.96%(图2)。
每公顷苦竹林0~90 cm土层土壤中植硅体碳储量为681.4 kg, 远大于地上部分植硅体碳总储量(83.7 kg), 其中表层土(0~10 cm土层)中储存75.3 kg(表2), 占总储量的11.05%。
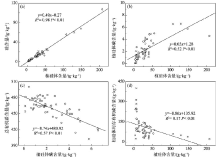
硅是地壳当中第二大元素, 其含量仅次于氧[22], 在碳循环中也起着重要的作用[23]。苦竹不同器官中硅的含量具有显著差异性, 在相同器官中, 不同竹龄的秆之间也存在显著的差异性(表1), 这些差异可能是植物的遗传特性和生长环境共同引起的[24]。植硅体作为硅在植物体内积淀后的一种存在形式, 在植物抗寒、抗逆等方面[20]具有重要的作用。自然生长的苦竹寿命在6 a左右[13], 研究发现4年生苦竹叶中植硅体含量最高(表1), 植硅体的含量并没有随着竹龄的增加而升高, 由此可以推断在苦竹生长的过程中随着竹龄的增加, 竹叶中植硅体的含量均会增加, 抵抗外界不利条件的能力也不断增强, 达到生命最旺盛的阶段以后即进入衰老阶段, 植硅体的含量随之降低。研究进一步对不同器官中的硅及植硅体含量进行分析, 两者之间存在极显著的相关关系 [R2= 0.98, P< 0.01, 图3(a)], 左昕昕等[25]对黍(Panicum miliaceum)、粟(Setaria italica)的研究, Li等[26]对湿地芦苇(Phragmites australis)的研究, Parr等[3]对经济竹林的研究及Song等[27]对中国草原的研究也表明了这一点, 说明植物体中植硅体的含量明显受到植物体对硅富集能力的影响。
植硅体封存有机碳是封存于植硅体中的有机碳相对于植硅体的总称[28], 植硅体封存有机碳和植硅体的含量共同决定着植物体中植硅体碳的含量, 不同植物之间植硅体封存有机碳的能力具有很大的差异[10], 已有研究表明竹类植物植硅体封存有机碳的含量[11]> 莎草> 小麦> 湿地植物[26]> 黍> 粟> 甘蔗。本研究对不同年龄段苦竹不同器官植硅体封存有机碳的含量进行分析, 发现相同竹龄不同器官中植硅体封存有机碳含量具有显著性差异(P= 0.05; 表1)。对各器官中硅、植硅体和植硅体封存有机碳进行分析, 发现无论是Si、植硅体还是植硅体封存有机碳含量在不同竹龄竹叶中均无显著差异性(P= 0.05; 表1), 而植硅体封存有机碳的含量在竹枝中具有显著差异性, 在秆中除植硅体含量以外均具有显著差异性(P= 0.05; 表1), 说明竹类植物植硅体封存有机碳的能力较强, 并且竹叶是积累储存Si、植硅体等物质差异最小的部位, 较大的差异存在于竹枝和秆中, 而传统研究在进行植硅体碳封存估测时仅把叶片考虑在内[3, 9, 10], 忽视了低含量高生物量的枝和秆部分, 因此在进行竹林植硅体碳汇研究时, 将竹枝和秆纳入研究范围将使结果更加准确。
植硅体碳形成于植硅体积淀的过程中[2], 植物体中植硅体碳的含量受多种因素影响。Li等[16]在对白洋淀芦苇的研究中指出, 植硅体碳含量与植物吸收利用二氧化碳速率有直接的关系; Song等[10]在中国不同森林类型植硅体碳封存估测的研究中提出, 植硅体碳的含量与总硅含量之间存在密切的联系, 并且以硅含量的3%作为计算植硅体封存有机碳的标准; 同时有关甘蔗[29]、小麦[30]、狗尾草[27]等诸多研究表明植物体内植硅体的含量与植硅体碳的含量之间不存在明显的相关关系。本研究对植物体内植硅体、植硅体碳、总有机碳和植硅体封存有机碳的含量进行分析发现, 植硅体与植硅体碳之间存在极显著的正相关关系 [R2= 0.52, P < 0.01, 图3(b)], 植硅体碳与总有机碳 [R2= 0.57, P < 0.01, 图3(c)] 及植硅体与植硅体封存有机碳 [R2= 0.17, P < 0.01, 图3(d)] 之间均存在明显的负相关关系, 这一结果与以前诸多学者的观点不尽相同, 原因可能是不同器官中植硅体、植硅体碳含量等具有明显的差异, 而已有的研究仅限于竹叶这单一的植物器官[20], 本研究中综合了植物的不同器官, 更能反映竹林生态系统中不同物质含量之间的相关关系, 为今后竹林植硅体碳汇研究提供科学依据。
有研究表明, 禾本科植物中稻亚科和竹亚科植物能固定较多的植硅体碳[31], 并且相同植物的不同器官植硅体碳封存能力有很大差别[20]。比较已有相关研究结果可以发现单位面积竹类植物植硅体碳封存能力远高于其他植物[10, 32], 本研究中通过对苦竹不同器官植硅体碳储量进行研究, 发现苦竹林竹叶中植硅体碳储量仅为14.6 kg· hm-2(图4), 而把竹枝和秆计算在内以后, 每公顷竹林植硅体碳储量达70.7 kg, 其中枝和秆中储存的植硅体碳占叶枝秆总储量的79.4%。已有研究认为在竹枝和秆被收获以后, 竹枝和秆中的植硅体碳也随着枝和秆一起被运离产地, 每年只有竹叶中的植硅体碳随竹叶凋落后进入并被封存于土壤中[33], 所以仅以竹叶中的植硅体碳计算植硅体碳储量和封存速率。但植硅体碳是一种非常稳定的有机碳, 一旦形成, 不论是否进入土壤均能够长期稳定存在, 有关竹林碳汇的研究中仅通过竹叶来计算植硅体碳储量存在一定误差。植硅体碳封存速率直接决定着竹林植硅体碳汇能力, 假如每年凋落的竹叶中植硅体碳均没有被人为或其他因素破坏, 且多年竹枝和秆中植硅体碳年封存量是相同的, 我们可以发现每年封存于竹叶、竹枝和竹秆中的植硅体碳分别为18.3、1.8和20.1 kg· hm-2· a-1, 每年通过竹叶封存的植硅体碳仅占地上部分总封存量的45.5%(图4)。可见, 竹枝和秆中植硅体碳含量虽然很低, 但由于生长迅速且生物量巨大[12], 无论是计算竹林植硅体碳的储量还是植硅体碳封存速率时竹枝和秆均是不可忽视的。
有研究表明, 土壤腐殖质层中的大量植硅体对硅循环有极大的影响[21], Cornelis等在研究中还提到过土壤可溶性硅主要由植硅体和铁氧化物表面吸附的可溶性硅组成[34]。本研究对林下土壤表层土(0~20 cm)总硅及植物可利用硅的含量进行分析, 发现土壤中总硅的含量并不能决定苦竹植硅体的含量, 植硅体的含量与土壤中植物可利用硅 [R2= 0.91, P< 0.05, 图5(a)] 而非总硅 [R2= 0.16, P> 0.05, 图5(b)] 的含量之间具有显著的相关关系。说明土壤中硅的存在形态有多种形式, 仅有很少一部分形态的硅可以被植物吸收利用[21], 而这部分硅的多少决定着植硅体的形成, 间接影响植物植硅体碳汇能力。
植硅体碳是植物细胞内原有的某些有机组分[35]。受植硅体外层硅化合物的保护, 植硅体碳可以在植物体降解后在土壤中累积长达数世纪之久, 在某些特殊的土层中植硅体碳含量甚至占到了该土壤总碳含量的82%[3]。对于林下土壤来说, 由于林下土壤0~5 cm土层直接接触植物凋落物, 又是提供有机物质分解转换主要场所[36]的特殊性, 土壤有机碳和植硅体碳含量均远高于其他土层[37]。本研究中也发现0~5 cm和5~10 cm土层中土壤有机碳和植硅体碳的含量均远高于其他土层, 并且随着土层深度的增加, 植硅体碳占土壤有机碳的比例也不断增加(图2), 这可能是由于深层土壤中的有机物质形成的时间比较长久, 大部分有机物质已经分解, 而植硅体碳非常稳定, 就使得随着土层深度的增加, 植硅体碳占土壤有机碳的比例逐渐增加[16]。进一步对各土层中植硅体碳储量进行计算发现, 每公顷苦竹林表层土(0~10 cm土层)中储存75.3 kg植硅体碳, 占总储量的11.05 %。尽管表层土中植硅体碳含量较高, 但植硅体碳储量并没有远高于其他土层。而每公顷苦竹林表层土(0~10 cm土层)中储存了28.08 t土壤有机碳, 占土壤有机碳总储量的22.8 %, 远高于其他各土层。说明表土中含有一部分不稳定的有机碳, 随着土层的加深, 只有一部分较稳定的有机碳最终积累在土壤中, 所以才会出现表层远高于下层土的现象, 而植硅体碳一旦形成即非常稳定, 在各土层中不会有很大的差别。同时通过对苦竹的研究我们发现经光合作用转化形成的总有机碳中仅0.59%、0.21%和0.28%以植硅体碳的形式分别存在于叶、枝和秆中, 假如能够通过人工措施提高植硅体碳在总有机碳中的比例, 增加植硅体碳封存速率, 将对于有效降低大气中CO2浓度具有重要的意义。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|